Възраждането на натриево-йонните батерии със стайна температура
Поради обилните запаси от натрий (Na) в земната кора и сходните физикохимични свойства на натрия и лития, базираното на натрий електрохимично съхранение на енергия има значителни обещания за широкомащабно съхранение на енергия и развитие на мрежата. Например, високотемпературни батерии с нулеви емисии за изследователска активност, базирани на Na/NiCl2 системи и високотемпературни Na–S клетки, които са успешни търговски случаи на стационарни и мобилни приложения, вече демонстрираха потенциала на натриевите акумулаторни батерии. Високата им работна температура от около 300 °C обаче причинява проблеми със сигурността и намалява ефективността на натриево-йонните батерии (SIB). Следователно SIB при стайна температура (RT) се считат широко за най-обещаващата алтернативна технология на LIB.
През историята на батериите през последните 200 години, изследванията върху SIBs се провеждаха пламенно рамо до рамо с развитието на LIB. Електрохимичната активност на TiS2 за литий и неговата осъществимост за съхранение на енергия беше представена за първи път през 70-те години на миналия век. След това откритие способността на Na йони да бъдат вмъкнати в TiS+2 беше осъзната в началото на 80-те години. С откриването на графита като евтин аноден материал с умерен капацитет за LIBs и неуспеха за интеркалиране на натриеви йони, бързото развитие на LIB настъпи през 90-те години, измествайки растежа в натриевата химия. След това, през 2000 г., наличието на съхранение на натрий в твърд въглерод (HC), което ще осигури енергиен капацитет, подобен на този на Li в графит, подмлади изследователския интерес към SIB.
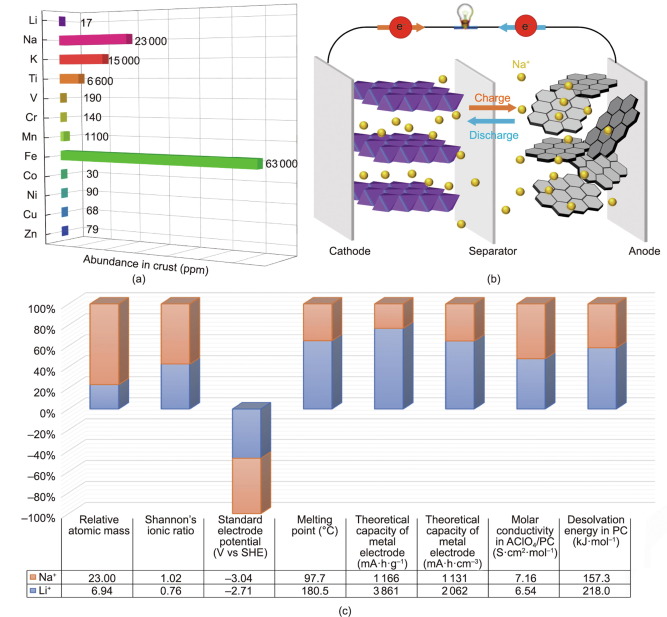
Сравнение на натриево-йонна батерия и литиево-йонна батерия
Възраждането на SIBs – съчетано с непрекъснато нарастващия натиск от липсата на наличност на резерви от литий и съответната ескалация на разходите – осигурява допълнителна стратегия към LIBs. SIBs спечелиха все по-голямо изследователско внимание, съчетано с фундаментални постижения в науката за материалите, в стремежа да се отговори на нарастващото навлизане на технологиите за възобновяема енергия. Клетъчните компоненти и механизмите на електрохимичната реакция на SIBs са основно идентични с тези на LIBs, с изключение на носителя на заряд, който е Na в единия и Li в другия. Основната причина за бързото разширяване на химията на SIB материалите се приписва на паралелите във физикохимичните свойства между двата алкални метала.
Първо, принципите на работа и клетъчната конструкция на SIBs са подобни на тези на търговските LIBs, макар и с Na, който служи като носител на заряд. В типичен SIB съществуват четири основни компонента: катоден материал (обикновено Na-съдържащо съединение); аноден материал (не е задължително да съдържа Na); електролит (в течно или твърдо състояние); и разделител. По време на процеса на зареждане натриевите йони се извличат от катодите, които обикновено са наслоени метални оксиди и полианионни съединения, и след това се вкарват в анодите, докато токът се движи през външна верига в обратна посока. При разреждане Na напуска анодите и се връща в катодите в процес, наричан „принципът на люлеещия се стол“. Тези прилики позволиха предварителното разбиране и бързия растеж на SIB технологията.
Освен това по-големият йонен радиус на Na носи своите предимства: повишена гъвкавост на електрохимичната положителност и намалена енергия на десолватация в полярни разтворители. По-голямата разлика в йонния радиус между Li и йоните на преходния метал обикновено води до провал на гъвкавостта на дизайна на материала. За разлика от това, базираната на натрий система позволява по-гъвкави твърди структури от системата, базирана на литий, и притежава огромна йонна проводимост. Типичен пример е β-Al2O3, за който интеркалирането на Na има идеалния размер и висока проводимост. Повече слоести оксиди на преходни метали с различни M+x+ начини на подреждане могат лесно да бъдат реализирани в система, базирана на натрий. По същия начин голямото разнообразие от кристални структури, които са известни за семейството на натриев йонен проводник (NaSICON), е много по-сложно от това на литиевите аналози. По-важното е, че много по-висока йонна проводимост може да бъде разрешена в съединенията на NaSICON, която далеч надвишава йонната проводимост в съединенията с литиево-йонен проводник (LiSICON).
Не на последно място, систематичните изследвания с различни апротонни полярни разтворители показват, че по-големият йонен радиус на Na причинява по-слаба енергия на десолватация. По-малкият Li има по-висока плътност на повърхностния заряд около ядрото от Na, когато и двата притежават една и съща валентност. Следователно Li е термодинамично стабилизиран чрез споделяне на повече електрони с молекулите на полярния разтворител. Тоест Li може да се класифицира като вид киселина на Люис. В резултат на това е необходима сравнително висока енергия на десолватация за силно поляризирания Li, което води до сравнително голямо съпротивление на трансфер, предизвикано от транспортирането на Li от течно състояние (електролит) към твърдо състояние (електрод). Тъй като енергията на десолватация е тясно свързана с кинетиката на трансфера, възникваща на интерфейса течност/твърдо вещество, относително ниската енергия на десолватация е значително предимство за проектиране на SIB с висока мощност.